醚键的断裂
正常的醚类化合物,由于性质上比较稳定,值得我们注意的化学反应并不多。在基础有机的学习中,主要就是酸性条件下 醚键断裂的反应。
做这个反应时,我们一般是将醚与卤化氢在酸性条件下混合加热,此时醚中会断开一根C-O键,分离成两部分,一半儿生成醇,另一半儿与 卤素结合得到卤代烃。当然如果HX过量,得到的醇与HX还可以进一步发生亲核取代,最终也得到卤代烃分子:
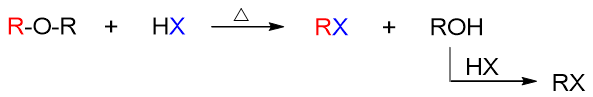
反应历程
从某种意义上看,这个醚键断裂的反应也可以视之为一个亲核取代,相当于来自于HX的亲核试剂X-取代了 原本醚中的离去基团RO-。当然,亲核取代可能存在SN1、SN2两种不同的历程,而醚键断裂的反应具体采取 何种历程,与醚中烃基的结构直接相关。
如若醚中氧两侧是伯烃基(如乙醚),则反应一般按SN2历程进行:

反之若氧两侧是叔烃基(如叔丁醚),则反应一般按SN1历程进行:
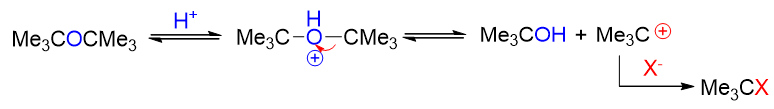
当然,由于生成了碳正离子,因此叔丁醚的反应中往往还会同时得到E1消除的产物2-甲基丙烯:
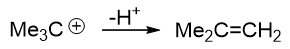
包括生成的叔丁醇,酸性加热条件下也会进而消除生成烯烃:
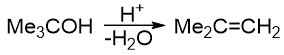
若醚中是仲烃基,情况则较复杂,视反应条件,SN1/SN2均有可能。
但不论是SN1还是SN2,我们也可以注意到,这个反应的第一步总是氧的质子化,形成醚的[钅羊]盐。这一点上和我们之前学习的醇的 很多反应类似,也是为了提高C-O键的极性便于其断开,同时也使得不易离去的RO-转变为易于离去的基团ROH。
不对称醚的断键方向
以上我们看到的都是结构对称的简单醚的情况。至于两个烃基不同的混合醚,醚键断裂时往往会存在区域选择性问题,主要断开哪根C-O键, 还是与反应历程相关。以下我们来看一些典型的案例。
- 例1:甲乙醚(80版命名)/乙甲醚(17版命名)的断键。
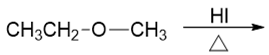
甲乙醚中,氧两侧一边是伯烃基,另一边是更小的甲基,我们很容易理解,它应当是按照SN2的历程进行反应,亲核试剂X-会主动进攻烃基引发C-O断键。既然是亲核试剂主动进攻,自然哪边位阻小哪边进攻更容易,因此这里主要的进攻位点将是甲基, 也是甲基与卤素结合形成碘甲烷,而乙基一侧连同氧原子,最终得到乙醇:
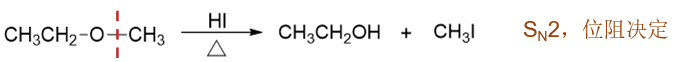
- 例2:甲基叔丁基醚(80版命名)/叔丁基甲基醚(17版命名)的断键。
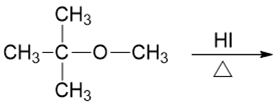
如果醚中含有叔烃基,我们实验中发现,一般情况下主要会按照SN1的历程进行反应,由叔烃基这侧断开C-O键形成较稳定的 叔碳正离子。即便像本例,另一个烃基是位阻很小的甲基,一般也不会走SN2历程。了解了这点,我们不难判断断键方向, 写出最终产物:
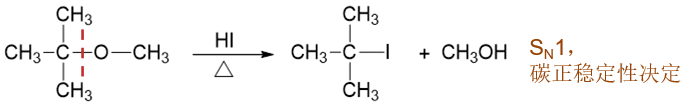
- 例3:苯甲醚(80版命名)/甲基苯基醚(17版命名)的断键。
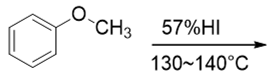
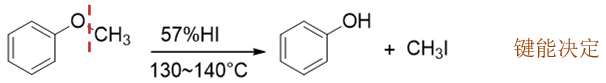
本例底物分子为一芳香醚。这里我们其实压根儿不用去判断反应机理究竟是SN1还是SN2了,注意到当前苯环与氧之间明显存在 共轭,这导致Ph-O键具有部分双键的性质,键能远高于Me-O键,很难断开。因此本反应中断键,只能是脂肪烃基于氧之间的 那一根:
- 例4:二苯醚。
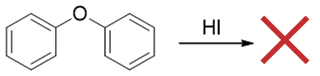
当前氧原子两侧都是苯环,两边都能形成共轭,键能较高,因此目前条件下都难以断开,不会发生醚键断裂的反应。
总之,醚键断裂的反应本身变化不多,在考试中比较容易出现的,也就是不对称醚的反应,大家掌握上述规律即可。