开链烷烃的物理性质
基础《有机化学》课程中,我们更关注化学性质,物理性质不算特别重要,大多数种类化合物的物理性质考试里也都不会涉及。 但烷烃的物理性质,尤其是熔沸点,非常有规律,因此考试中常会出现。这两个物理性质的变化规律对于开链烷烃而言既有联系,也有不同。
判断一组开链烷烃熔沸点的高低,基本有两个原则:
同系物:结构类似(直、支链状况相仿),看碳原子数目(也就是分子量),愈大者熔沸点一般愈高;
同分异构体:碳原子数相同,看支链多少,一般支链越多熔沸点越低,但支链如果对称性特别高,熔点(而非沸点)反而要比支链者高(和分子晶体晶胞堆积紧密程度有关)。
尤其是这第二条原则,考试当中出现频率极高,特别小心对称性高的支链烷烃。
如一组很典型的例子:
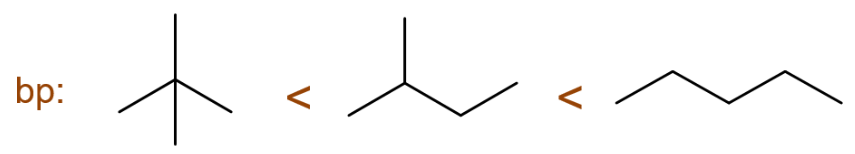
沸点比较简单,支链越多越低
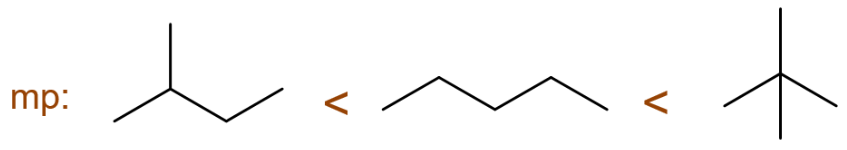
熔点还需要小心分子对称性
至于为什么说2,2-二甲基丙烷(新戊烷)对称性高, 看看 分子模型 应该就知道了, 其实就相当于把甲烷正四面体顶点的四个氢替换成甲基,对称性也就和甲烷相仿。
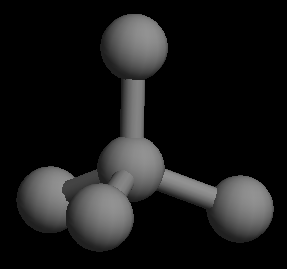
2,2-二甲基丙烷分子立体结构(隐氢)
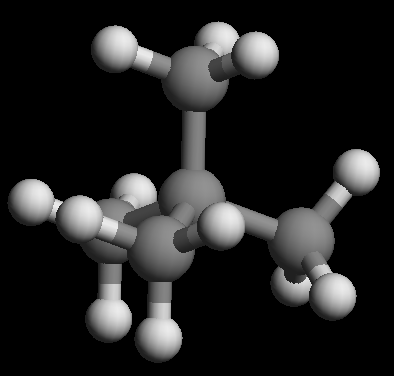
2,2-二甲基丙烷分子立体结构(显氢)