取代苯酚的酸性
酚是一类具有明显酸性的有机化合物,我们知道它的酸性一般较水、醇都来得高。而酚中最常见的,无疑是苯酚。在苯酚的基础上, 通过苯环上的亲电取代反应,我们也很容易得到一系列的苯酚衍生物,而这些衍生物通常也都是具有酸性的。当然,由于 取代的基团不同,各种苯酚衍生物的酸性也有差异。在基础有机的学习中,我们也应当掌握判断苯酚衍生物酸性 强弱的方法。
在基础有机化学中判定化合物的酸性强弱,其实有个比较固定的方法。我们知道根据质子酸碱理论,有酸性的化合物在溶剂中 可以解离出质子,存在下图的解离平衡:
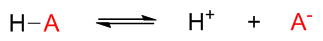
在上面的解离平衡中,不同的酸性化合物,都是解离出质子,只是负离子有差异而已。而这个负离子的稳定性越强,明显 平衡就越容易向右偏,解离出的质子浓度当然会越高,相应的,该化合物的酸性也就越强。因此我们这儿可以得到个明显的 结论:化合物酸性与解离质子后形成负离子的稳定性成正比。
对于取代苯酚而言,它的酸性我们也可以用同样的方式去判断。如下图所示,不同结构的取代苯酚, 解离质子后都能得到结构类似的苯氧基负离子(图中Y为苯环上的取代基团,取代位置不定):
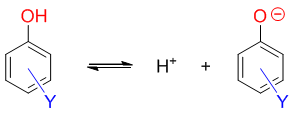
同样,取代苯酚的酸性就与生成的负离子稳定性直接相关。至于右侧的负离子稳定性如何,很大程度上又可以根据 取代基团Y的性质确定:如果Y具有吸电子效应,可以把电子往自己身边拉,无疑会使得氧原子上电子云密度下降,原本 较集中的负电荷将得到分散,这种取代负离子的稳定性将高于无取代的苯氧基负离子。反之若Y具有给电子效应,把电子向 苯环、向氧原子方向推,无疑会使氧上负电荷更为集中,稳定性将较无取代的苯氧基负离子下降。
总之一个基本规律:连接吸电子基,取代苯酚酸性将较苯酚上升;反之连接给电子基,取代苯酚酸性将下降。
依据以上的原则,我们来看几个实例。
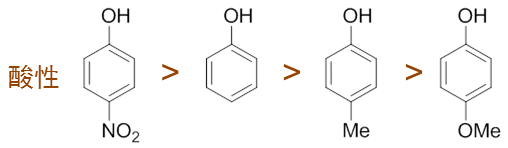
- 例:请判断如下化合物的酸性次序。
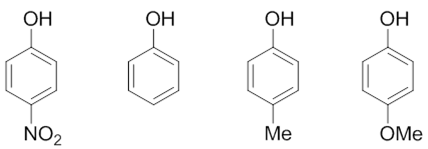
我们假设这四个分子各自解离出酚羟基上的质子,将得到下图中四种负离子。通过取代基的电性效应,这四种负离子的稳定性 次序我们不难判断。其中第一个,对硝基苯氧基负离子,明显硝基强吸电子(-I/-C),稳定性将较苯氧基负离子更强。而第三个 对甲基苯氧基负离子,由于甲基给电子(+I),无疑稳定性将较苯氧基负离子来得弱。至于最后的对甲氧基苯氧基负离子, 由于对位甲氧基给电子能力较甲基更强(-C>+I),因此在四种负离子中它的稳定性应当最差。
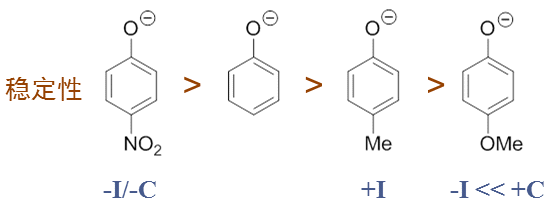
判定了负离子稳定性,质子解离之前各取代苯酚的酸性也就随之确定,次序与稳定性相同:
- 例:请判断如下化合物的酸性次序。
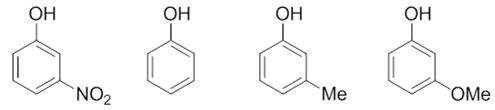
与前例类似,只不过我们当前把几个取代基团从酚羟基的对位移到了间位。
表面看起来,取代基团甭管是在对位还是间位,给/吸电子的性质应该不会发生改变,这四个分子的酸性次序应当与前例类似。但实测 情况略显奇怪:
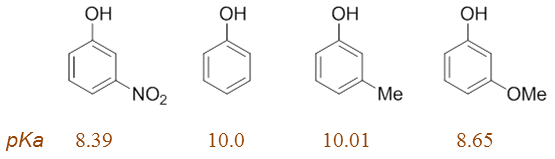
我们发现,原本看起来应当酸性最弱的间甲氧基苯酚,实测酸性反而比间甲基苯酚甚至无取代的苯酚都来得更强。似乎这里甲氧基 变成了一个吸电子基团?事实上,这与共轭效应的区域性有关系。
我们在基础有机中接触的电性效应主要就两种:诱导效应与共轭效应。诱导效应基本不存在区域性,分子里甭管什么位置,都能受到 取代基诱导效应的影响(当然,距离越远,影响越弱)。而共轭效应则大不相同,由于种种原因,分子中的某些特定位置,往往受到 的影响更为强烈,另一些位置往往又几乎感觉不到共轭效应的存在,存在明显的区域性。
对于取代苯衍生物而言,取代基团共轭效应影响比较大的是其自身的邻、对位。相反,取代基团的间位,则几乎不受共轭效应的影响。 本例中间甲氧基苯酚酸性强于苯酚,实际就是这种区域性的结果。
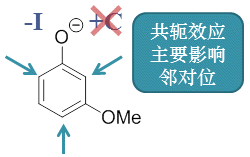
甲氧基的两种电性效应相反,-I/+C,而通常情况下我们说+C>-I, 当它连接在苯环旁侧是,整体上应该是个中等强度的给电子基团。但注意目前间甲氧基苯氧基负离子中,负电中心氧原子刚好处于甲氧基 间位,而这个位置偏偏又基本不受甲氧基的给电子共轭效应的影响。于是,如下图所示,没了共轭,只剩下诱导,当前的氧负离子端就基本只能感受到 甲氧基的吸电子诱导效应,负电荷得以分散,这种负离子的稳定性也就相应地上升了,间甲氧基苯酚的酸性也就因之较苯酚更强。
类似的,间硝基苯酚中其实也存在相同的情况,酚羟基处于硝基间位,同样基本不受硝基共轭效应的影响,也只能感受到诱导效应。好在 硝基本身的诱导效应也是强吸电子,它依然是这四个分子中酸性最高的一个。
备注
不单是取代苯酚,很多芳香衍生物中,共轭效应的区域性都会对化合物的性质造成影响,我们也需要特别留神。
- 例:请判断如下两个化合物的酸性次序。
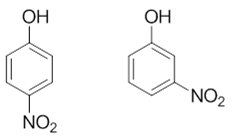
都是硝基取代,一个对位,一个间位。明显本例中也存在共轭效应区域性的影响。
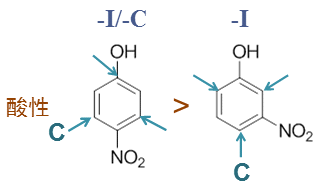
如下图所示,对于对硝基苯酚,明显羟基侧能够受到硝基两种电性效应(-I、-C)的共同影响。而间硝基苯酚, 羟基只能感受到硝基的诱导效应(-I)。两相比较,-I/-C的加和明显吸电子程度要大于单独的-I, 于是我们可以断言,对硝基苯酚的酸性将较间硝基苯酚更强。
- 例:请判断如下化合物的酸性次序。
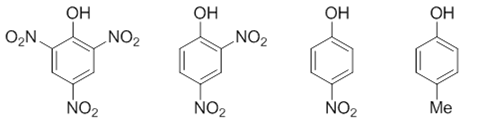
本例较简单,苯环旁侧要么连接甲基,只有给电子诱导效应,不分区域;要么连接硝基,硝基还都处于羟基邻对位,共轭或诱导效应 都可以影响到羟基。此外,不同分子中,硝基的数目不同,而我们也很容易想象,电性效应是具备叠加性的,2,4,6-三硝基苯酚 形成的负离子由于三个硝基吸电子,稳定性自然强于2,4-二硝基苯酚得到的负离子。依次类推,这一系列分子酸性次序如下图所示:
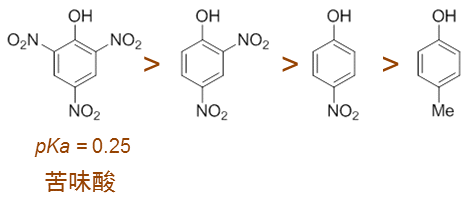
其中,2,4,6-三硝基苯酚由于三个强吸电子硝基共同的影响,它的酸性相当之高,pKa=0.25,已经接近很多无机酸了。因此这个 分子的俗名我们称为苦味酸——不叫酚,直接称为酸了。
关于取代苯酚的酸性,我们大致就看这么几个典型例子。这种通过负离子稳定性,通过取代基团电性效应判定酸性方法相当普适, 我们在后面的学习中还会遇到类似的情况。