羧酸衍生物的化学反应
羧酸衍生物(除腈外)结构中都含有酰基官能团,因而表现出相似的化学性质,其反应机理也大致相同,只是在反应活性上有所差异。
酰基与羰基的区别
酰基:X、O或N的未共用电子对与酰基的π键形成p-π共轭,使得C-Y键的键长较典型键长有所缩短。酰基碳原子带有电正性,但是的吸电子能力不如羰基碳原子。
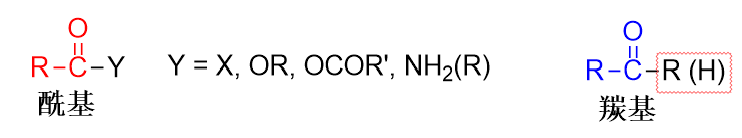
能发生如下反应:

接受亲核试剂(如:水、醇、胺、格氏试剂等)的进攻,发生亲核取代(先加成,后消除)。
酰基的吸电子效应导致羧酸衍生物的α-H显示一定的酸性,在碱性条件下可形成碳负离子,发生与碳负离子有关的反应。
羧酸衍生物还可以发生还原反应。
羰基:羰基碳原子与氧原子的p轨道侧面重叠形成π键,由于氧原子电负性较大,故羰基中的π键是极化的,表现为羰基碳原子带正电荷。
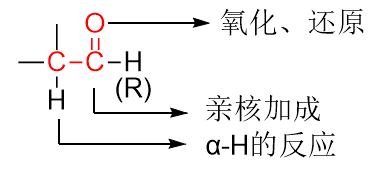
正电荷的碳原子易被亲核试剂进攻发生亲核加成。
由于羰基的吸电子效应,导致醛酮α-H具有一定活性。
羰基化合物易发生氧化还原反应。
这三类反应中,羧酸衍生物的亲核取代(水解、醇解、氨解)反应具有一定的共性;羧酸衍生物的还原反应与羧酸类似。涉及碳负离子的反应将在下一章详细讨论。
羧酸衍生物的水解
所有的羧酸衍生物均可发生水解反应而生成羧酸,反应通式如下:
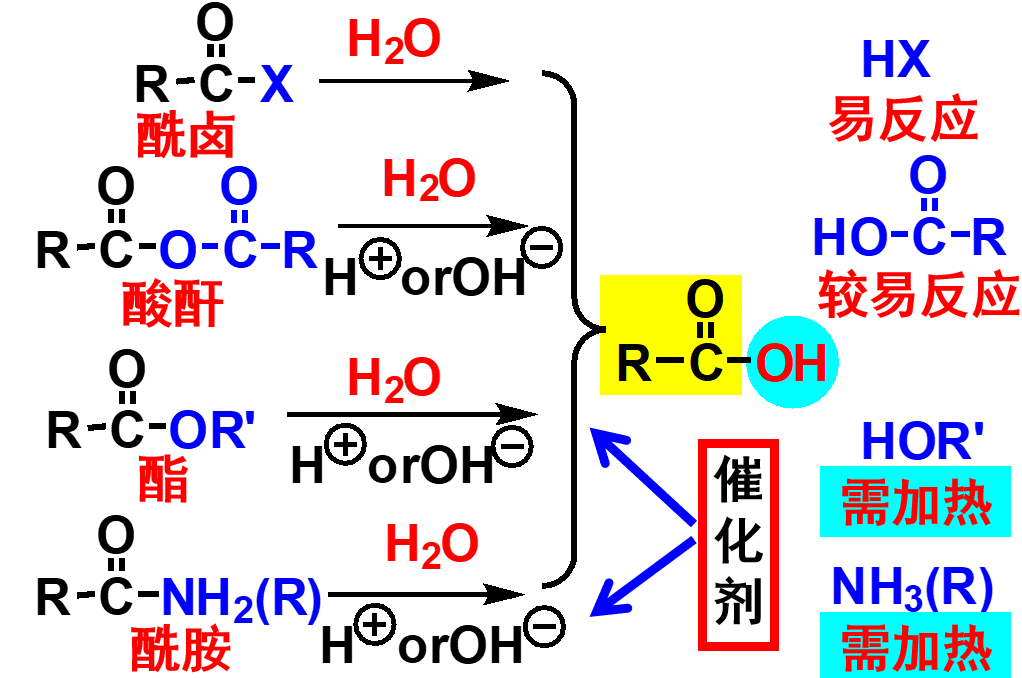
酰卤、酸酐:易水解,一般没用处;
酯:酸或碱催化并加热。酸催化反应可逆;碱催化不可逆,碱通常需要过量;
酰胺:酸或碱催化,加热回流。均不可逆;
腈:酸或碱催化,加热回流。均不可逆;
反应活性:酰氯>酸酐>酯>酰胺(腈)。
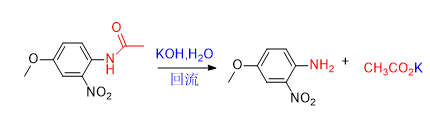
例如:下面的例子中N-(4-甲氧基-2-硝基苯基)乙酰胺在氢氧化钾水溶液中回流,酰胺键发生断裂,生成相应的胺和羧酸盐。
酯水解的反应机理
酯在酸催化下水解反应是可逆的;在碱催化下反应是不可逆的,因为水解生成的羧酸与碱作用生成羧酸负离子,羧酸负离子的羰基正电性下降,不能接受醇的亲核进攻,你反应不再发生,故酯在见过两的条件下可彻底水解。
酯碱性条件下的水解
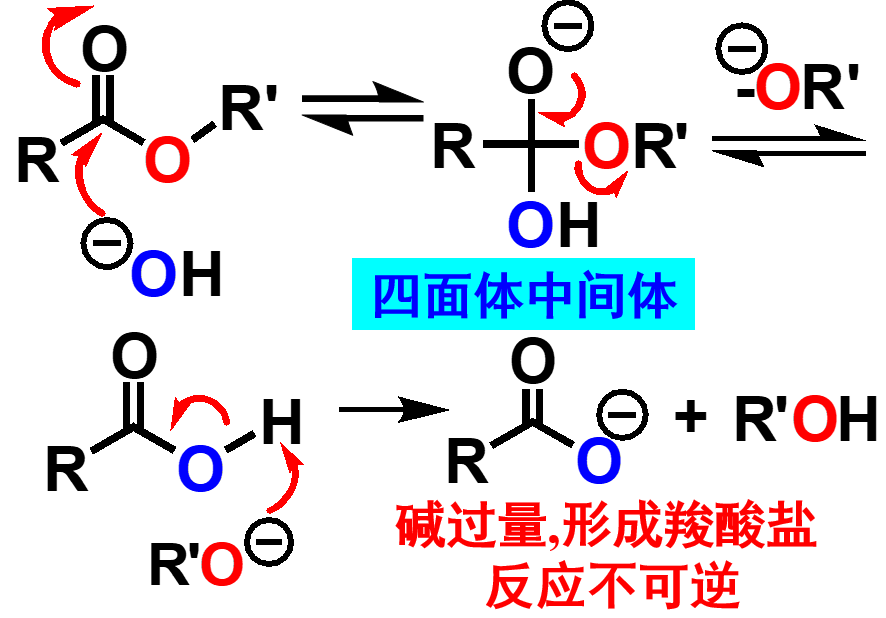
氢氧根的亲核性较强,首先进攻酰基碳,发生亲核加成,生成四面体中间体,随后发生消除,失去烷氧基负离子,生成羧酸。因为反应条件为碱性,生成的羧酸与碱发生酸碱中和,最终生成羧酸盐,因此反应是不可逆的。酯碱性条件下的水解反应为亲核取代,经历加成-消除过程。一般适用甲醇、伯醇、仲醇的酯。 那么,酯在碱性条件下的水解,断键的位置在酰氧键还是烷氧键呢? 下面的同位素实验证明,酯的水解是酰氧断裂: .. image:: ../../images/C12-KeyPoints/ReactionOfcarboxylicacidderivatives07.png
影响碱水解反应速率的因素
由上面使的反应机理可知,反应经历四面体中间体,因此中间体越稳定,反应速率越快;反应的第一步为亲核加成,如果亲核试剂和酰基旁边的空间位阻较大,反应速率会降低。
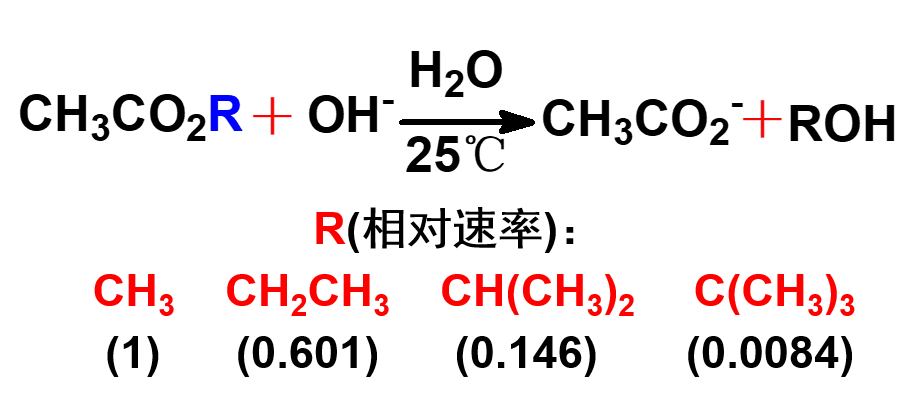
上面的例子中,随着R基团的增大,反应速率逐渐降低。
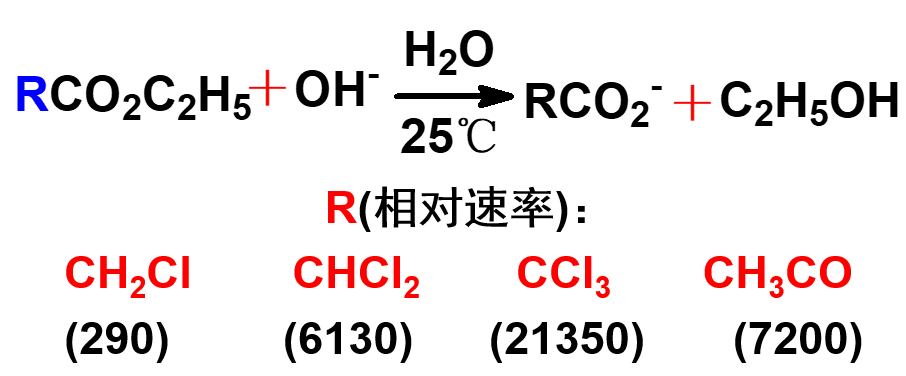
上面的例子中,随着R基团上吸电子基团的增多,反应速率加快。 例如:请比较下列酯在碱性条件下水解的速度:
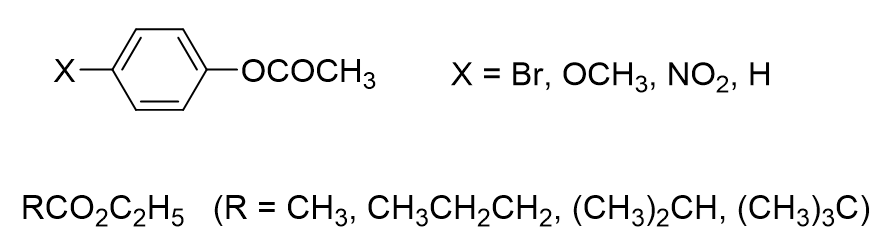
酯水解反应速率的快慢与酰基的空间位阻和电性有关,此题目中X基团分别为溴、甲氧基、硝基和氢,并连在苯环的对位,溴与苯环相连为弱吸电子基团,甲氧基主要体现给电子效应,硝基则为强吸电子基团,根据电性因素,基团的吸电子效应越强,酰基的电正性越强,越容易接受亲核试剂的进攻,所以,本题不同化合物水解速率的大小为-硝基>-Br>H>-OCH3。
酯酸性条件下的水解
酯水解也可在酸性条件下进行。羧酸的伯、仲醇酯水解时也是以酰氧键断裂的方式进行的。
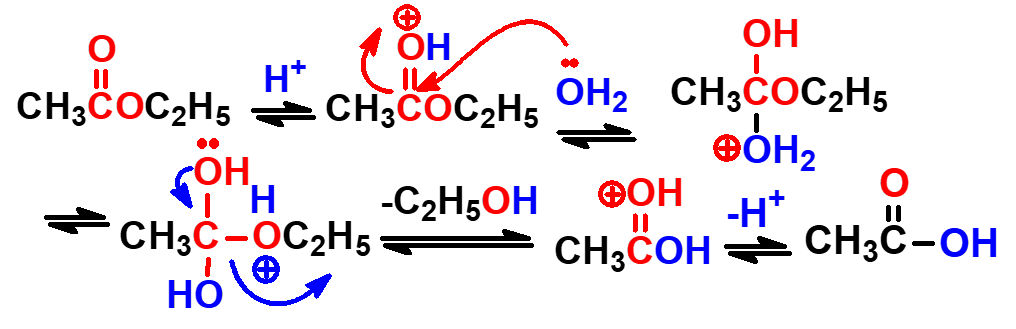
首先是酯分子中的羰基氧原子质子化,使羰基碳原子的正电性增加,有利于弱亲核试剂水对其进攻而生成四面体正离子中间体,然后质子转移到烷氧基氧原子上,再消除弱碱性的醇分子而生成羧酸。酸催化下酯水解的反应速率也与中间体的稳定性有关,电性效应对水解速率的影响不如在碱催化水解中打,而空间位阻对反应速率的影响较大。 叔醇酯在酸催化下水解时,由于空间位阻较大,且易生成相对稳定的碳正离子,所以水解反应按照烷氧基断裂的方式进行。
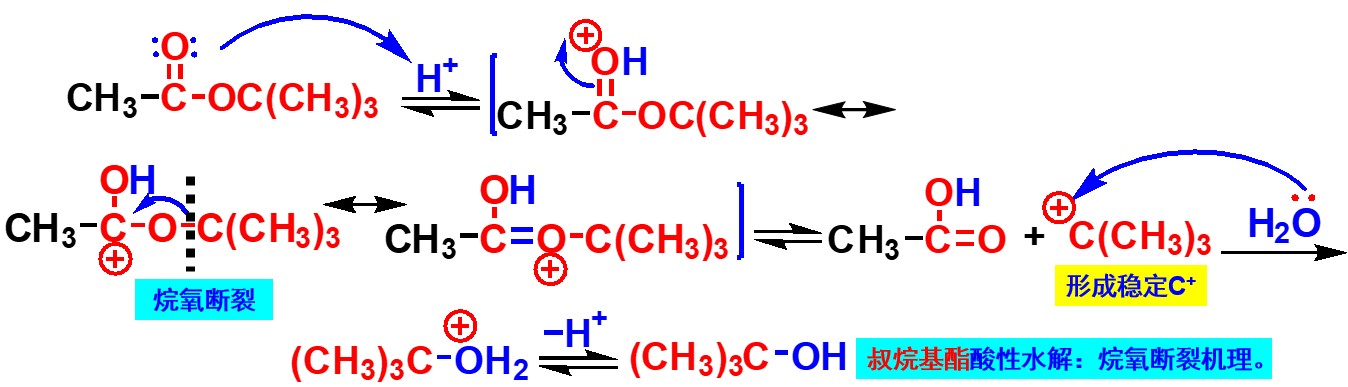
例如:请写出下列反应的主要产物:
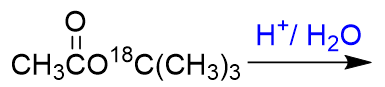
题目中的酯为乙酸叔丁酯,同位素标记在烷氧基上,基于以上分析,叔醇酯水解断裂的位置在烷氧键,因此产物为:
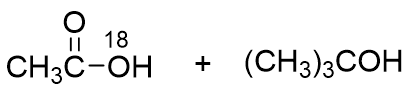
羧酸衍生物的醇解
羧酸衍生物醇解生成酯,此反应是合成酯类化合物的重要方法。
酰卤的醇解
酰卤很容易与醇或酚反应生成酯,通常用来制备难以直接通过酯化反应得到的酯。对于活性较弱的酰卤或叔醇和酚,需要在碱性条件下进行,碱可促进该反应。
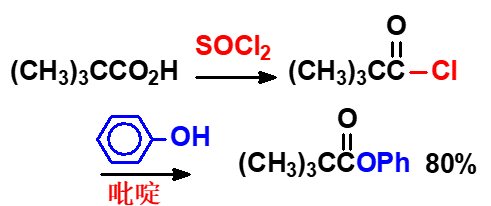
2,2-二甲基丙酸的空间位阻较大,苯酚也不能直接与羧酸成酯,所以,原料先于氯化亚砜反应生成酰氯,以此来活化反应底物,随后与苯酚反应,可以80%的收率得到目标产物。
酸酐的醇解
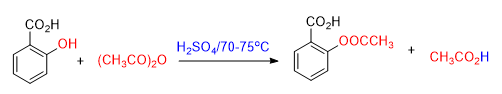
酸酐的醇解较酰卤温和,反应可用少量酸或碱催化,也是制备酯的常用方法。例如:解热镇痛药阿司匹林就是以水杨酸为原料,在硫酸催化下与乙酸酐作用制得的。
酯的醇解
在酸或碱催化下,酯与醇反应,酯分子中的烷基被醇分子中的烷氧基置换,称为酯的醇解。反应通式如下:
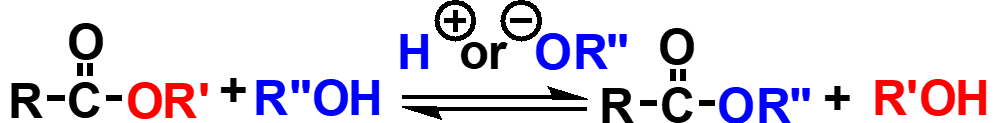
这是一个酯转变为另一个酯的过程,又称为酯交换反应。酯交换反应常用来制备难以合成的酯(如:酚酯或烯醇酯)或从沸点低的酯合成沸点高的酯。
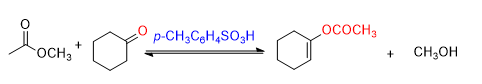
在上面的例子中,环己酮在酸性条件下发生烯醇化,变成环己烯醇,然后发生酯的醇解,生成最终的目标产物。
例如:请写出下列反应的主要产物:
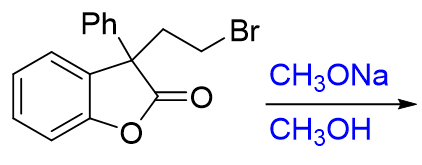
该反应涉及酯在碱性条件下的醇解。具体反应机理如下:
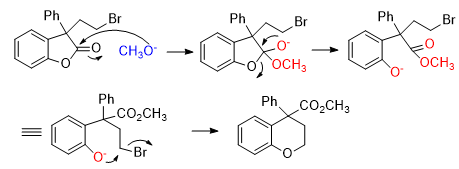
首先甲氧基负离子进攻酰基,发生亲核加成反应,生成四面体中间体,随后发生消除,生成酚氧负离子;酚氧负离子作为亲核试剂进攻与溴相连的中心碳原子,发生分子内亲核取代,最终生成目标产物。
羧酸衍生物的氨解
羧酸衍生物与氨或胺作用生成酰胺,这是制备酰胺的常用方法。由于氨/胺的亲核性比水、醇强,所以羧酸衍生物的氨解反应比水解、醇解更加容易。
酰卤的氨解
酰卤与氨/胺可迅速形成酰胺,反应通常在碱性条件下进行。
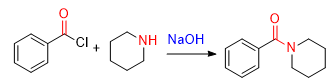
分子量较小的酰卤,氨解反应剧烈,大量放热,生成HX与NH3作用也放热,通常需要冷却和稀释;反应中加热有机或无机碱,以吸收生成的酸。
酸酐的氨解
酸酐的反应活性比酰卤稍弱,反应较温和。因此,酸酐氨解的反应速率比酰卤慢。
环状酸酐与氨/胺反应,则开环生成酰胺酸的铵盐,酸化后生成酰胺酸,那为什么不生成双酰胺呢?
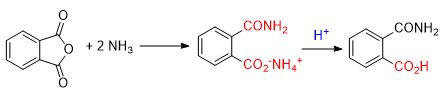
酸酐先发生氨解,生成单酰胺和羧酸,因氨过量,羧酸与氨生成铵盐,如果要进一步生成酰胺,则需要加热,脱去一分子水而形成酰胺。
酯的氨解
酯与氨/胺基氨的衍生物(如:肼、羟胺)发生氨解生成酰胺或酰胺衍生物。由于氨/胺的亲核性比醇强,所以酯的氨解不需要加催化剂。例如:
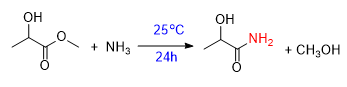
例:请完成下列反应
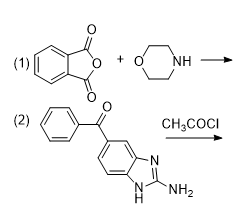
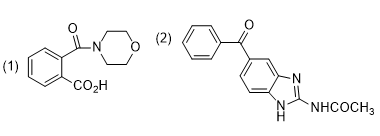
第一题考察的知识点为酸酐的氨解,这里吗啉中氮原子的亲核性大于氧原子,所以反应发生的是氨解;第二题其中一个底物是酰氯,另一个底物中有多个氨基,考察氨基的亲核性强弱,五元杂环中有两个氮原子,一个是吡啶型氮原子,一个是吡咯型氮原子(见杂环化合物),还有一个氨基,这里氨基的亲核性较强,因此,此位置的氨基发生亲核取代,生成酰胺,具体参看如下答案。
羧酸衍生物的与有机金属化合物的反应
与格氏试剂的反应
各类羧酸衍生物均能与格氏试剂反应,首先进行加成-消除反应生成酮,酮进一步与格氏试剂反应生成叔醇。
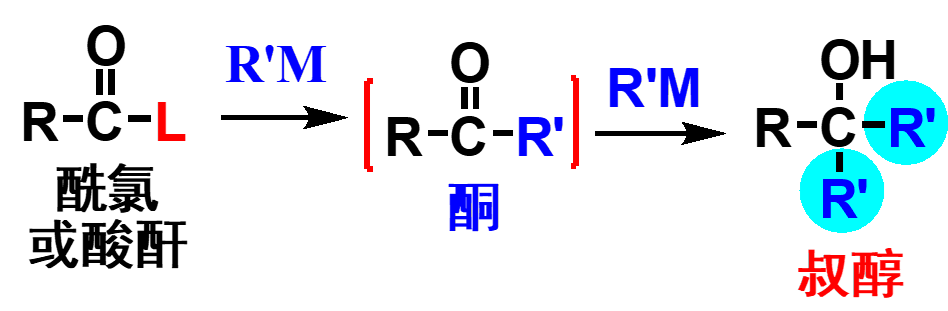
合成中较为常见的为酯与格氏试剂的反应,以制备α-碳原子上至少连有两个相同烃基的叔醇;若用甲酸酯与格氏试剂反应,则生成对称的仲醇;内酯也能发生类似的反应,产物为二元醇。
例如:
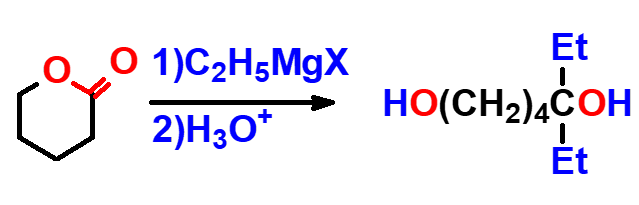
这种内酯是如何与格氏试剂反应的呢?格氏试剂本质上提供烷基负离子,它是很强的亲核试剂。因此,首先乙基负离子进攻酯羰基,发生亲核加成,随后消除烷氧基负离子,得到中间体1,中间体1中有羰基,羰基的亲核加成反应活性大于酯羰基,随后酮羰基进一步与乙基负离子发生亲核加成反应,最后经过水解而得到目标产物,请参看下列的反应机理:
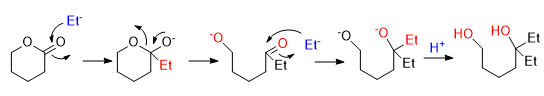
总体而言,此部分内容的知识点相似度较高,均发生的是亲核取代反应(先加成-后消除),经历的中间体为四面体中间体,亲核取代的反应速率受到空间位阻和电性效应的影响。羧酸衍生物发生亲核取代反应一般活性顺序为:酰卤>酸酐>酯>酰胺(腈)。